中国组织工程研究 ›› 2013, Vol. 17 ›› Issue (20): 3687-3691.doi: 10.3969/j.issn.2095-4344.2013.20.011
• 组织构建实验造模 experimental modeling in tissue construction • 上一篇 下一篇
构建吗啡依赖条件性位置厌恶模型大鼠伏隔核壳区相关基因的表达
张景丹1,李文强1,宋秀花1,娄百玉1,石玉中1,李 毅2
- 1河南省精神病医院,河南省新乡市 453002
2武汉市精神卫生中心,湖北省武汉市 430022
Expressions of related genes in the shell of accumbens nuclei when constructing a rat model of chronic morphine-induced conditioned place aversion
Zhang Jing-dan1, Li Wen-qiang1, Song Xiu-hua1, Lou Bai-yu1, Shi Yu-zhong1, Li Yi2
- 1 Henan Provincial Mental Hospital, Xinxiang 453002, Henan Province, China
2 Wuhan Mental Health Center, Wuhan 430022, Hubei Province, China
摘要:
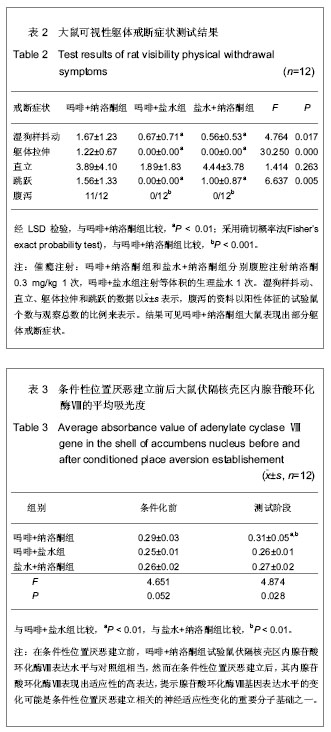
背景:腺苷酸环化酶Ⅷ涉及促进吗啡耐受、戒断和强化性能,对晚期长时程增强效应、长时程记忆和对应激的适应等可塑性变化中发挥重要的作用。 目的:基于慢性吗啡依赖大鼠纳洛酮催瘾戒断建立的条件性位置厌恶动物模型,观察在条件性位置厌恶建立前后,与成瘾密切相关脑区伏隔核壳区内腺苷酸环化酶Ⅷ基因表达的适应性变化。 方法:选用清洁级雄性SD大鼠,设模型组(吗啡+纳洛酮组)、吗啡+盐水组和盐水+纳洛酮组。模型组采用连续6.5 d慢性吗啡腹腔注射10 mg/kg,纳洛酮一次催瘾注射0.3 mg/kg,同时与条件性位置训练箱搭配建立大鼠条件性位置厌恶模型,对照组依模型组对照注射等体积生理盐水。在条件性位置厌恶建立前后,采用免疫组织化学方法检测伏隔核壳区内腺苷酸环化酶Ⅷ基因的表达水平。 结果与结论:条件性位置厌恶建立前,3组腺苷酸环化酶Ⅷ在伏隔核壳区表达水平差异无显著性意义(F=4.651,P=0.052);条件性位置厌恶建立后,吗啡+纳洛酮组腺苷酸环化酶Ⅷ在伏隔核壳区(F=4.874, P=0.028)内表达水平显著高于吗啡+盐水组和盐水+纳洛酮组。结果提示,伏隔核壳区内腺苷酸环化酶Ⅷ水平可能是调节阿片类物质戒断所致厌恶动机的关键因子之一;腺苷酸环化酶Ⅷ基因表达水平的变化可能是条件性位置厌恶建立相关的神经适应性变化的重要分子基础之一。
中图分类号: